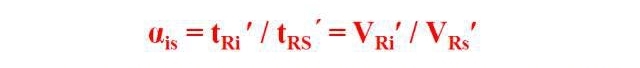La cromatografía, también conocida como "análisis cromatográfico", "cromatografía", es un método de separación y análisis, que tiene una gama muy amplia de aplicaciones en química analítica, química orgánica, bioquímica y otros campos.
El fundador de la cromatografía es el botánico ruso M. Tsvetter.En 1906, el botánico ruso Zvetter publicó los resultados de su experimento: para separar los pigmentos vegetales, vertió extracto de éter de petróleo que contenía pigmentos vegetales en un tubo de vidrio que contenía polvo de carbonato de calcio y lo eluyó con éter de petróleo de arriba a abajo.Debido a que diferentes pigmentos tienen diferentes capacidades de adsorción en la superficie de las partículas de carbonato de calcio, durante el proceso de lixiviación, diferentes pigmentos descienden a diferentes velocidades, formando así bandas de diferentes colores.Se separaron los componentes del pigmento.Llamó a este método de separación cromatografía.
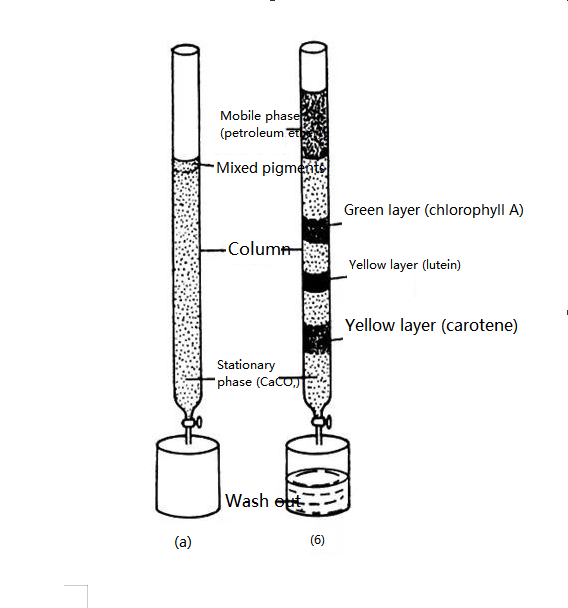
Representación esquemática de un experimento de separación de pigmentos de hojas de plantas.
Con el continuo desarrollo de los métodos de separación, cada vez más sustancias incoloras se convierten en objeto de separación, la cromatografía también perdió gradualmente el significado de "color", pero el nombre todavía se utiliza en la actualidad.
Clasificación cromatográfica
La esencia de la cromatografía es un proceso en el que las moléculas que se van a separar se dividen y equilibran entre la fase estacionaria y la fase móvil.Las diferentes sustancias se dividen de manera diferente entre las dos fases, lo que hace que se muevan a diferentes velocidades con la fase móvil.Con el movimiento de la fase móvil, los diferentes componentes de la mezcla se separan entre sí en la fase estacionaria.Dependiendo del mecanismo, se puede dividir en una variedad de categorías.
1, según la clasificación del estado físico de dos fases.
Fase móvil: cromatografía de gases, cromatografía líquida, cromatografía de fluidos supercríticos
Fase estacionaria: gas-sólido, gas-líquido;Líquido-sólido, líquido-líquido
2, según la forma de clasificación de fase estacionaria.
Cromatografía en columna: cromatografía en columna empaquetada, cromatografía en columna capilar, cromatografía en columna microempaquetada, cromatografía preparativa
Cromatografía plana: cromatografía en papel, cromatografía en capa fina, cromatografía de membrana polimérica
3, clasificado según el mecanismo de separación.
Cromatografía de adsorción: los diferentes componentes se separan según sus capacidades de adsorción y desorción en adsorbentes.
Cromatografía de partición: Los diferentes componentes se separan según su solubilidad en el disolvente.
Cromatografía de exclusión molecular: según el tamaño del tamaño molecular de la separación. En cromatografía de intercambio iónico: diferentes componentes de la afinidad por la separación con resina de intercambio iónico.
Cromatografía de afinidad: Separación utilizando la presencia de una afinidad específica entre macromoléculas biológicas.
Electroforesis capilar: los componentes se separaron según las diferencias en movilidad y/o comportamiento de partición.
La cromatografía quiral se utiliza para la separación y análisis de fármacos quirales, que se pueden dividir en tres categorías: método de reactivo de derivatización quiral;Método de aditivo de fase móvil quiral;Método de resolución de fase estacionaria quiral.
Terminología básica para cromatografía.
Las curvas obtenidas trazando las señales de respuesta de los componentes después de la detección de la separación cromatográfica frente al tiempo se denominan cromatogramas.
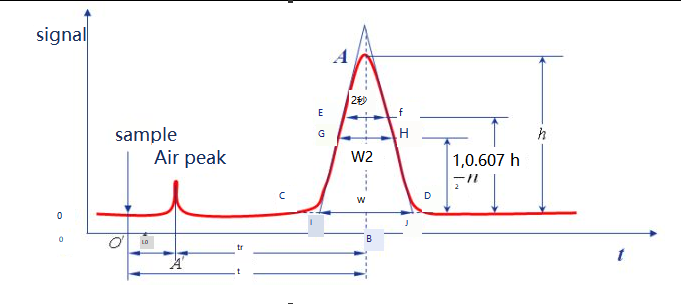
Base:Bajo ciertas condiciones cromatográficas, la curva de la señal generada cuando solo la fase móvil pasa a través del sistema detector se llama línea base, como se muestra en la línea ot.Cuando la condición experimental era estable, la línea de base era una línea paralela al eje horizontal.La línea base refleja el ruido del instrumento, principalmente el detector, a lo largo del tiempo.
Altura del pico:la distancia vertical entre el punto máximo cromatográfico y la línea base, denotada por h, como se muestra en la línea AB'.
Ancho de región:El ancho de la región del pico cromatográfico está directamente relacionado con la eficiencia de separación.Hay tres métodos para describir el ancho del pico cromatográfico: desviación estándar σ, ancho del pico W y FWHM W1/2.
Desviación estándar (σ) :σ es la media distancia entre los dos puntos de inflexión en la curva de distribución normal, y el valor de σ indica el grado de dispersión de los componentes lejos de la columna.Cuanto mayor sea el valor de σ, más dispersos estarán los componentes del efluente y peor será el efecto de separación.Por el contrario, los componentes del efluente se concentran y el efecto de separación es bueno.
Ancho de pico W:Los puntos de intersección a ambos lados del pico cromatográfico se utilizan como líneas tangentes y la intersección en la línea de base se denomina ancho de pico o ancho de línea de base, que también se puede expresar como W, como se muestra en la Figura IJ.Según el principio de distribución normal, se puede demostrar que la relación entre el ancho del pico y la desviación estándar es W = 4σ.
W1/2:El ancho del pico a la mitad de la altura del pico se llama FWHM, como se muestra para la distancia de GH.W1/2=2,355σ, W=1,699W1/2.
W1/2, W se derivan de σ y se utilizan para calcular las áreas de los picos además de medir el efecto de la columna.La medición FWHM es más conveniente y más utilizada.
breve resumen
A partir de la curva cromatográfica de flujo máximo de salida, se pueden lograr los siguientes objetivos:
a, el análisis cualitativo se realizó según el valor de retención de los picos cromatográficos.
b, análisis cuantitativo basado en el área o pico del pico cromatográfico
C. La eficiencia de separación de la columna se evaluó según el valor de retención y el ancho del pico cromatográfico.
La fórmula de cálculo involucrada en la cromatografía.
1. Valor de retención
El valor de retención es un parámetro que se utiliza para describir el grado en que se retiene un componente de la muestra en la columna y se utiliza como indicador de la caracterización cromatográfica.Su método de representación es el siguiente:
Tiempo de retención tR
Hora de la muertetM
Ajustar el tiempo de retención tR'=tR-tM
(Tiempo total transcurrido en fase estacionaria)
Volumen de retención
VR=tR*F.(independiente de la velocidad de la fase móvil)
Volumen muerto
VM=tM*Fc
(El espacio no ocupado por la fase estacionaria en la ruta de flujo desde el inyector hasta el detector)
Ajustar el volumen de retención VR'=t'R*fc
2. Valor de retención relativo
El valor de retención relativo, también conocido como factor de separación, relación de coeficiente de partición o factor de capacidad relativa, es la relación entre el tiempo de retención ajustado (volumen) del componente probado y el tiempo de retención ajustado (volumen) del estándar en determinadas condiciones cromatográficas.

Se utilizaron valores de retención relativa para eliminar la influencia de ciertas condiciones operativas, como el caudal y la pérdida de fijación, sobre los valores de retención.El estándar en el valor de retención relativo puede ser un componente de la muestra analizada o un compuesto añadido artificialmente.
3. Índice de retención
El índice de retención es el índice de retención de la sustancia i que se va a analizar en una solución fija X. Se seleccionan dos n-alanos como sustancias de referencia, una de las cuales tiene un número de carbonos N y la otra tiene N+n.Su tiempo de retención ajustado es t 'r (N) y t 'r (N+n), respectivamente, de modo que el tiempo de retención ajustado t 'r (i) de la sustancia i a ensayar está exactamente entre ellos, es decir, t'r (norte).
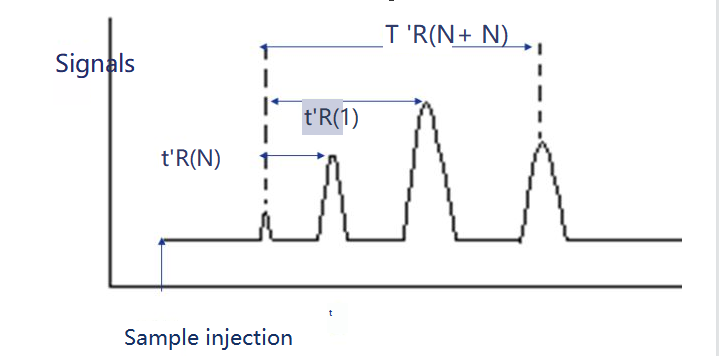
El índice de retención se puede calcular de la siguiente manera.
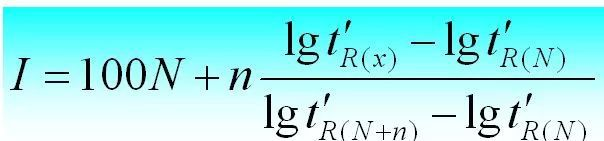
4. Factor de capacidad (k)
En equilibrio, la relación entre la masa de un componente en la fase estacionaria y la fase móvil (m), se denomina factor de capacidad.La fórmula es la siguiente:
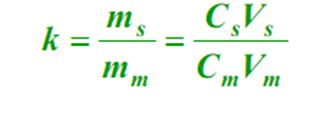
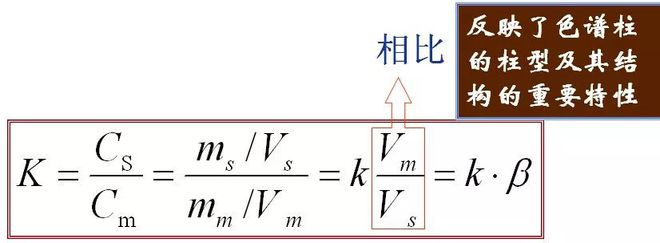
5. Coeficiente de partición (K) En equilibrio, la relación entre la concentración de un componente en la fase estacionaria (s) y la fase móvil (m), denominada coeficiente de partición.La fórmula es la siguiente.

La relación entre K y k:
Refleja el tipo de columna y su nudo, propiedades importantes de la estructura.
breve resumen
Relación entre valor de retención y factor de capacidad y coeficiente de partición:
La separación cromatográfica se basa en la diferencia en la capacidad de adsorción o disolución de cada componente en una muestra relativa fija, que puede expresarse cuantitativamente mediante el tamaño del valor del coeficiente de partición K (o factor de capacidad k).
Los componentes con fuerte capacidad de adsorción o disolución tienen un gran coeficiente de partición (o factor de capacidad) y un largo tiempo de retención.Por el contrario, los componentes con adsorción o solubilidad débil tienen un coeficiente de partición pequeño y un tiempo de retención corto.
Teoría básica de la cromatografía.
1. Teoría de la bandeja
(1) Propuesta: teoría termodinámica
Comenzó con el modelo de placa de torre propuesto por Martin y Synge.
Columna de fraccionamiento: en el plato para varios tiempos de equilibrio gas-líquido, según el punto de ebullición de las diferentes separaciones.
Columna: Los componentes están equilibrados mediante múltiples particiones entre las dos fases y separados según diferentes coeficientes de partición.
(2) Hipótesis
(1) Hay muchas bandejas en la columna y los componentes pueden alcanzar rápidamente el equilibrio de distribución dentro del intervalo de la bandeja (es decir, la altura de la bandeja).
(2) La fase móvil entra en la columna, no de forma continua sino pulsante, es decir, cada paso es un volumen de columna.
(3) Cuando se añadió la muestra a cada plato de columna, se pudo despreciar la difusión de la muestra a lo largo del eje de la columna.
(4) El coeficiente de partición es igual en todas las bandejas, independientemente de la cantidad de componentes.Es decir, el coeficiente de partición es constante en cada tabán.
(3) Principio
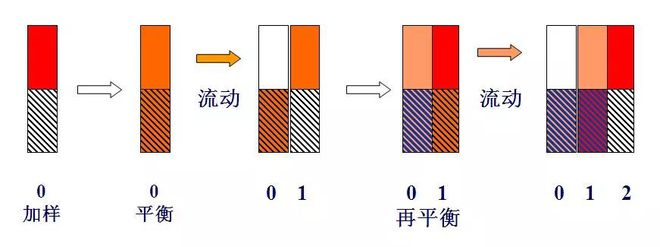
Diagrama esquemático de la teoría de la bandeja.
Si un componente de unidad de masa, a saber, m=1 (por ejemplo, 1 mg o 1 μg), se añade a la bandeja nº 0, y después del equilibrio de distribución, porque k=1, a saber, ns=nm, nm=ns=0,5.
Cuando un volumen de placa (lΔV) de gas portador ingresa a la placa 0 en forma de pulsación, el gas portador que contiene el componente nm en la fase gaseosa es empujado a la placa 1. En este momento, el componente ns en la fase líquida de la placa 0 y el componente nm en la fase gaseosa de la placa 1 se redistribuirá entre las dos fases.Por lo tanto, la cantidad total de componentes contenidos en la placa 0 es 0,5, en la que las fases gaseosa y líquida son 0,25 cada una, y la cantidad total contenida en la placa 1 también es 0,5.Las fases gaseosa y líquida también fueron 0,25.
Este proceso se repite cada vez que se pulsa un nuevo volumen de gas portador en la placa hacia la columna (consulte la tabla a continuación).
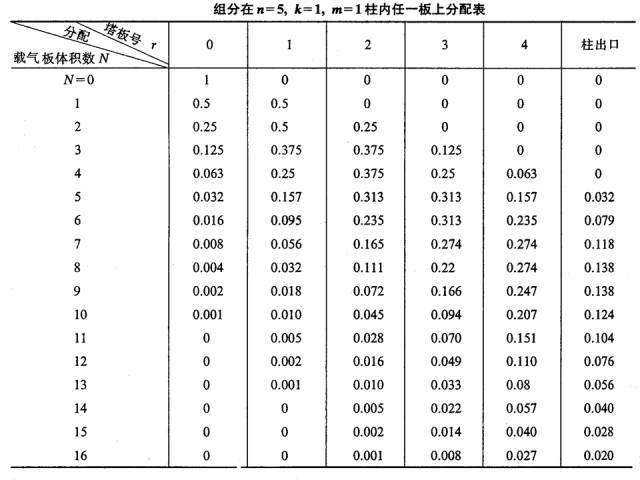
(4) Ecuación de la curva de flujo de salida cromatográfica

σ es la desviación estándar, es el tiempo de retención, C es la concentración en cualquier momento,
C, es la concentración de inyección, es decir, la cantidad total de componentes (área del pico A).
(5) parámetros de eficiencia de la columna
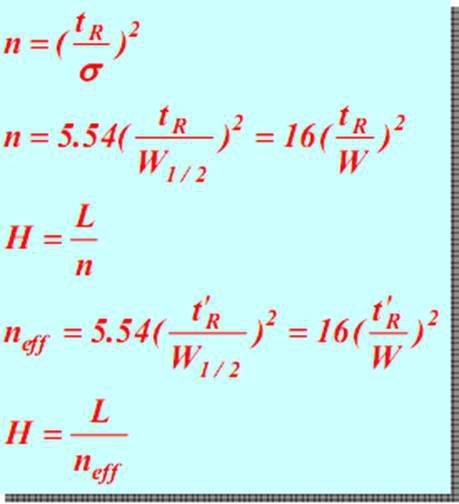
A un tR constante, cuanto menor sea W o w 1/2 (es decir, el pico más estrecho), mayor será el número de platos teóricos n, menor será la altura teórica del plato y mayor será la eficiencia de separación de la columna.Lo mismo ocurre con la teoría efectiva de la bandeja Neff.Por tanto, el número teórico de platos es un índice para evaluar la eficiencia de las columnas.
(5)Características y deficiencias
> Ventajas
La teoría de la bandeja es semiempírica y explica la forma de la curva de salida.
Se ilustran los procesos de partición y separación de los componentes.
Se propone un índice para evaluar la eficiencia de la columna.
> Limitaciones
Los componentes realmente no pueden alcanzar el equilibrio de distribución en las dos fases:
No se puede ignorar la difusión longitudinal de los componentes en la columna:
No se consideró la influencia de diversos factores cinéticos en el proceso de transferencia de masa.
La relación entre el efecto de la columna y la velocidad del flujo de la fase móvil no se puede explicar:
No está claro qué factores principales afectan el efecto columna.
Estos problemas se resuelven satisfactoriamente en la teoría de tasas.
2. Teoría de tarifas
En 1956, el académico holandés VanDeemter et al.absorbió el concepto de teoría de la bandeja y combinó los factores cinéticos que afectan la altura de la bandeja, propuso la teoría cinética del proceso cromatográfico - teoría de la velocidad y derivó la ecuación de VanDeemter.Considera el proceso cromatográfico como un proceso dinámico de no equilibrio y estudia la influencia de factores cinéticos en el ensanchamiento del pico (es decir, efecto columna).
Posteriormente, Giddings y Snyder et al.propuso la ecuación de velocidad de cromatografía líquida (es decir, ecuación de Giddings) basada en la ecuación de VanDeemter (más tarde llamada ecuación de velocidad de cromatografía de gases) y de acuerdo con la diferencia de propiedades entre líquido y gas.
(1) Ecuación de Van Deemter
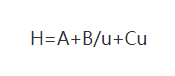
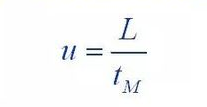
Donde: H: es la altura del tablero
A: coeficiente del término de difusión en remolino
B: coeficiente de término de difusión molecular
C: coeficiente del término de resistencia a la transferencia de masa
(2) Ecuación de Giddings
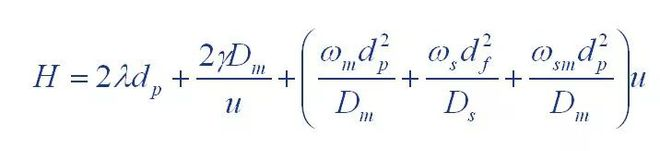
Análisis cuantitativo y cualitativo.
(1) Análisis cualitativo
El análisis cromatográfico cualitativo consiste en determinar los compuestos representados por cada pico cromatográfico.Dado que diversas sustancias tienen valores de retención definidos en determinadas condiciones cromatográficas, el valor de retención puede utilizarse como índice cualitativo.Actualmente, varios métodos cromatográficos cualitativos se basan en valores de retención.
Sin embargo, diferentes sustancias pueden tener valores de retención similares o idénticos bajo las mismas condiciones cromatográficas, es decir, los valores de retención no son excluyentes.Por tanto, es difícil caracterizar una muestra completamente desconocida basándose únicamente en los valores de retención.Si se comprende la fuente, la naturaleza y el propósito de la muestra, se puede hacer un juicio preliminar de la composición de la muestra y se pueden usar los siguientes métodos para determinar el compuesto representado por el pico cromatográfico.
1. Control cualitativo mediante sustancias puras
En determinadas condiciones cromatográficas, una sustancia desconocida sólo tiene un tiempo de retención definido.Por lo tanto, lo desconocido puede identificarse cualitativamente comparando el tiempo de retención de la sustancia pura conocida en las mismas condiciones cromatográficas con el tiempo de retención de la sustancia desconocida.Si las dos son iguales, la sustancia desconocida puede ser una sustancia pura conocida;De lo contrario, lo desconocido no es la sustancia pura.
El método de control de sustancias puras sólo es aplicable a la sustancia desconocida cuya composición se conoce, cuya composición es relativamente simple y cuya sustancia pura se conoce.
2. Método del valor de retención relativo
El valor de retención relativo α, se refiere al ajuste entre el componente i y los materiales de referencia. Relación de valores de retención:
Solo cambia con el cambio de temperatura del fijador y de la columna, y no tiene nada que ver con otras condiciones operativas.
A una determinada temperatura de fase estacionaria y de columna, los valores de retención ajustados del componente i y de la sustancia de referencia s se miden respectivamente y luego se calculan según la fórmula anterior.Los valores de retención relativa obtenidos se pueden comparar cualitativamente con los valores correspondientes en la literatura.
3, agregando sustancias conocidas para aumentar el método de altura máxima
Cuando hay muchos componentes en la muestra desconocida, los picos cromatográficos obtenidos son demasiado densos para identificarlos fácilmente mediante el método anterior, o cuando la muestra desconocida sólo se utiliza para el análisis del elemento especificado.
"Primero se hace un cromatograma de una muestra desconocida y luego se obtiene otro cromatograma añadiendo una sustancia conocida a la muestra desconocida".Para tales sustancias se pueden conocer componentes con alturas de pico elevadas.
4. Conservar el método cualitativo del índice.
El índice de retención representa el comportamiento de retención de sustancias sobre fijadores y actualmente es el índice cualitativo más utilizado y reconocido internacionalmente en GC.Tiene las ventajas de una buena reproducibilidad, un estándar uniforme y un coeficiente de temperatura pequeño.
El índice de retención sólo está relacionado con las propiedades de la fase estacionaria y la temperatura de la columna, pero no con otras condiciones experimentales.Su precisión y reproducibilidad son excelentes.Siempre que la temperatura de la columna sea la misma que la de la fase estacionaria, se puede aplicar el valor publicado en la literatura para la identificación y no es necesario utilizar el material puro para comparar.
(2)Análisis cuantitativo
Bases para la cuantificación cromatográfica:
La tarea del análisis cuantitativo es encontrar los cientos de componentes en la muestra mixta.
Contenido fraccionado.La cuantificación cromatográfica se basó en lo siguiente: cuando las condiciones de operación eran consistentes, se
La masa (o concentración) del componente medido está determinada por la señal de respuesta proporcionada por el detector.
Es proporcional.A saber:
Bases para la cuantificación cromatográfica:
La tarea del análisis cuantitativo es encontrar los cientos de componentes en la muestra mixta.
Contenido fraccionado.La cuantificación cromatográfica se basó en lo siguiente: cuando las condiciones de operación eran consistentes, se
La masa (o concentración) del componente medido está determinada por la señal de respuesta proporcionada por el detector.
Es proporcional.A saber:
1. Método de medición del área de pico
El área del pico son los datos cuantitativos básicos proporcionados por los cromatogramas, y la precisión de la medición del área del pico afecta directamente los resultados cuantitativos.Se utilizaron diferentes métodos de medición para picos cromatográficos con diferentes formas de pico.
Es difícil encontrar el valor exacto del invierno en un análisis cuantitativo:
Por un lado, debido a la dificultad de medir con precisión el volumen absoluto de inyección; por otro lado,
El área del pico depende de las condiciones cromatográficas y la tira cromatográfica debe mantenerse cuando se mide el valor.
No es posible ni conveniente hacer lo mismo.E incluso si puedes hacerlo bien
El valor exacto, también porque no existe una norma unificada y no se puede aplicar directamente.
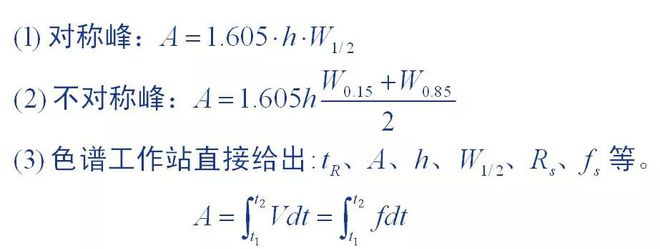
2.Factor de corrección cuantitativa
Definición de factor de corrección cuantitativa: cantidad de componentes que ingresan al detector (m)
La relación entre su área de pico cromatográfico (A) o altura de pico () es una constante de proporcionalidad (,
La constante de proporcionalidad se denomina factor de corrección absoluta del componente.
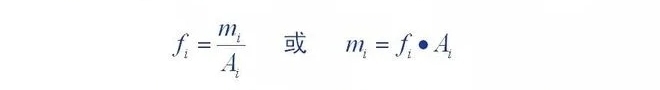
Es difícil encontrar el valor exacto del invierno en un análisis cuantitativo:
Por un lado, debido a la dificultad de medir con precisión el volumen absoluto de inyección; por otro lado,
El área del pico depende de las condiciones cromatográficas y la tira cromatográfica debe mantenerse cuando se mide el valor.
No es posible ni conveniente hacer lo mismo.E incluso si puedes hacerlo bien
El valor exacto, también porque no existe una norma unificada y no se puede aplicar directamente.
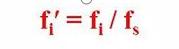
Es decir, el factor de corrección relativo 'de un componente es el componente y el material de referencia s
La relación de los factores de corrección absolutos.
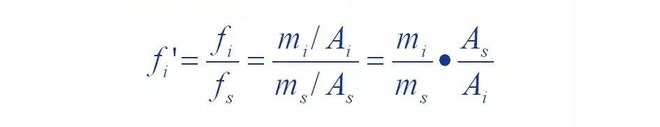
Se puede observar que el factor de corrección relativo es cuando la calidad del componente versus el estándar.
Cuando la sustancia s es igual, el área del pico del material de referencia es el área del pico del componente
Múltiple.Si algún componente tiene masa m y área de pico A, entonces el número de f'A
Los valores son iguales al área del pico del material de referencia con una masa de.En otras palabras,
Mediante el factor de corrección relativo, se pueden separar las áreas de pico de cada componente
Convertida al área del pico del material de referencia igual a su masa, luego la relación
El estándar está unificado.Este es el método normalizado para calcular el porcentaje de cada componente.
La base de la cantidad.
Método de obtención del factor de corrección relativo: los valores del factor de corrección relativo sólo se compararon con
La medida no está relacionada con el estándar y el tipo de detector, sino con la franja de operación.
No importa.Por lo tanto, los valores se pueden recuperar de las referencias de la literatura.si el texto
Si no encuentra el valor deseado en la oferta, también puede determinarlo usted mismo.Método de determinación
Método: una cierta cantidad de la sustancia medida, diez materiales de referencia seleccionados → elaborados en una determinada concentración
Se midieron las áreas de los picos cromatográficos A y As de los dos componentes.
Esa es la fórmula.
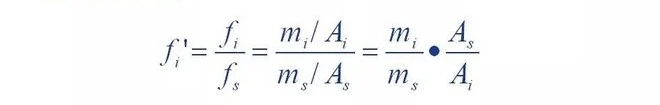
3. Método de cálculo cuantitativo
(1) Método de normalización de área
La suma del contenido de todas las fracciones libres de picos se calculó como 100% para la cuantificación.
El método se llama normalización.Su fórmula de cálculo es la siguiente:
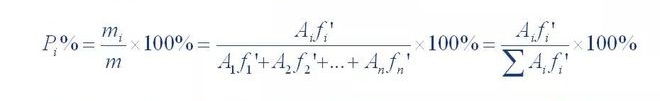
Donde P,% es el contenido porcentual de los componentes probados;A1, A2... An es el componente 1. El área del pico de 1~n;f'1, f'2... f'n es el factor de corrección relativo para los componentes 1 a n.
(2) método estándar externo
El método de comparación cuantitativa entre la señal de respuesta del componente que se va a probar en la muestra y el componente puro que se va a probar como control.
(3) Método estándar interno
El llamado método de estándar interno es un método en el que se agrega una cierta cantidad de sustancia pura a la solución estándar de la sustancia analizada y a la solución de muestra como estándar interno, y luego se analiza y determina.
(3)método de adición estándar
El método de adición estándar, también conocido como método de adición interna, consiste en agregar una cierta cantidad de (△C)
La referencia de la sustancia de prueba se agregó a la solución de muestra a analizar y la prueba se agregó al ensayo.
El pico de la solución de muestra después de la sustancia fue mayor que el de la solución de muestra original
El incremento del área (△A) se utilizó para calcular la concentración de la sustancia en la solución de muestra.
Contenido (Cx)
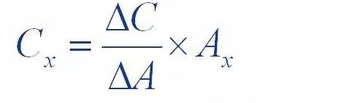
Donde Ax es el área del pico de la sustancia a medir en la muestra original.

Hora de publicación: 27 de marzo de 2023